塼懱僔儞僠儗乕僔儑儞僇僂儞僞偺恑曕
昅幰偑LSC偵弶傔偰弌夛偭偨偺偼1961擭5寧棷妛愭偺暷崙偺尋媶強偵偍偄偰偱偁偭偨丏偍偦傜偔丆LSC傪巊偭偨嵟弶偺擔杮恖偺堦恖偱偁傠偆丏崱擔丆LSC偼嵟傕晛媦偟偨曻幩慄應掕憰抲偱偁傞偑丆儐乕僓乕偼偦偺尨棟傪棟夝偣偢丆嵟嬤偺婡夿惈擻偺恑曕傪僼儖偵妶偐偝側偄傑傑巊偭偰偄傞嫲傟偑偁傞丏抪偢偐偟側偑傜丆昅幰帺恎傕MD偵娭傢傞傑偱偼LSC偺嵟嬤偺恑曕偵偮偄偰柍抦偱偁偭偨丏傑偢丆LSC偺尨棟偲嵟嬤偺恑曕偵偮偄偰弎傋傞丏
LSC偺尨宆偼3偮偺攇崅慖暿婍 (discriminator) 1,2,3乮慖暿揹埑偺掅偄懁偐傜乯偲榐悢婍偐傜側傝丆偁傜偐偠傔忦審愝掕偝傟偨discriminator 1偲2偱宍惉偝傟偨僠儍僱儖乮A僠儍僱儖乯偱3H傪丆discriminator 2偲3偱宍惉偝傟偨僠儍僱儖乮B僠儍僱儖乯偱14C 傪寁悢偡傞巇慻傒偵側偭偰偄偨丏奜晹慄尮偵懳偡傞寁悢傪巜昗偵偟偰僋僄儞僠儞僌傪曗惓偡傞曽朄偑奐敪偝傟丆LSC偼堦婥偵晛媦偟偨丏尰栶拞丆LSC偼丆帋椏傪僶僀傾儖偵嵦傝丆僔儞僠儗乕僞傪壛偊丆憰抲偵憰揢偟丆寁悢忦審傪偁傜偐偠傔愝掕偟偰僗僞乕僩儃僞儞傪墴偟偰偍偗偽丆梻挬偵偼dpm抣偑僾儕儞僩傾僂僩偝傟偰偄傞丆偼側偼偩庤偺偐偐傜側偄婡夿偱偁傞偲偄偆擣幆偟偐側偐偭偨丏
偦偺屻丆揹嶼婡偺晛媦偵偮傟偰LSC傕儅儖僠僠儍僱儖壔偝傟偨丏尰嵼偱偼偲傝偁偊偢寁悢張棟偟偰慡忣曬傪揹嶼婡偵婰壇偝偣丆攇崅僗儁僋僩儖傪尒偰寁悢偺嵟揔撉庢傝忦審傪慖傇偙偲偑偱偒傞傛偆偵側偭偨丏偙偺偙偲偼丆寁悢僨乕僞偺夝愅偵嬌傔偰戝偒側儊儕僢僩傪傕偨傜偟偨丏偡側傢偪丆尨宆偱偼寁悢奐巒帪偵偟偐偱偒側偐偭偨寁悢忦審偺愝掕偑丆寁悢張棟屻偵嵟揔撉庢傝忦審傪try and error偱慖戰偱偒傞傛偆偵側偭偨偙偲傪堄枴偟偰偄傞丏側偍丆儅儖僠僠儍僱儖壔偵敽偭偰丆A僠儍僱儖丆B僠儍僱儖偲屇傫偱偄偨偺偼偦傟偧傟3H僂僀儞僪僂丆14C僂僀儞僪僂偲屇傇傋偒偱偁傞偙偲傪昅幰偼巜揈偟偨乮6乯丏
挿偄娫丆堦庬偺曻幩慄寁悢憰抲偲偟偰尒側偝傟偰偒偨LSC偼丆偦偺塸岅柤liquid scintillation spectrophotometer偑帵偡傛偆偵,壗愮僠儍僱儖偲偄偆崅偄僄僱儖僊乕暘夝擻傪帩偮丆暘岝婍偲偟偰偺婡擻傕偁傢偣旛偊偨曻幩慄寁悢憰抲偱偁傞偙偲傪LSC儐乕僓乕偼擣幆偡傞傋偒偱偁傞丏尰嵼丆 LSC偺僨乕僞偼椺奜側偔寁悢抣偩偗偑採帵偝傟偰偄傞偑丆偙傟偼丆媧岝搙暘愅偱偄偆媧岝搙偩偗傪採帵偟偰偄傞偙偲偵憡摉偡傞丏BG帋椏傪娷傔戙昞揑側帋椏偵偮偄偰偼兝慄攇崅僗儁僋僩儖傪採帵偡傞偙偲偵傛偭偰寁悢僨乕僞偺怣棅惈傪堦抜偲崅傔傞偙偲偑偱偒傞丏
Low BG LSC偺峔惉
Fig. 2偵偼斈梡宆LSC偲Low BG LSC偺峔惉傪帵偟偨丏

Fig. 2 Block diagrams of a conventional LSC and Low BG LSC
寁悢帋椏偼僶僀傾儖偵嵦傜傟丆僔儞僠儗乕僞偵梟偐偟丆PMT偺娫偵抲偐傟傞丏14C偺夡曄偵傛偭偰曻弌偝傟偨兝棻巕偼寀岝懱暘巕偲徴撍偟偰寀岝傪敪偡傞丏偙偺寀岝傪PMT偺岝揹柺偱庴偗丆揹巕憹暆偟偰1偮偺寁悢偲偟偰庢傝弌偡偺偑LSC偺婎杮尨棟偱偁傞丏
14C偺兝夡曄偵傛偭偰敪惗偡傞岝巕偺悢偼丆偦偺兝慄偺僄僱儖僊乕偲僔儞僠儗乕僞偺寀岝岠棪偵傛偭偰寛傑傝丆慜偵夝愢偟偨傛偆偵暯嬒偟偰300屄偖傜偄偲尒愊傕傜傟傞丏偙傟傜偺岝巕偑巐曽敧曽偵曻幩偝傟傞丏 PMT偺岝揹柺偑僶僀傾儖傪朷傓棫懱妏傪10%偲偡傞偲丆PMT偺岝揹柺偵偼30屄偺岝巕偑擖幩偟丆揹巕乮堦師岝揹巕乯傪曻弌偝偣傞偙偲偵側傞丏堦師岝揹巕偼PMT偵傛偭偰揹巕憹暆偝傟丆1偮偺寁悢偲偟偰庢傝弌偝傟傞丏
尨棟偼娙扨偱偁傞偑丆幚梡揑側寁悢憰抲偵偡傞偵偼2偮偺岺晇偑昁梫偱偁偭偨丏偦偺戞1偼擬嶨壒thermal noise偵婲場偡傞BG傪偄偐偵掅偔偡傞偐偱偁偭偨丏嵟弶偲傜傟偨庤抜偼丆PMT偺擬嶨壒偼壏搙偵斾椺偟偰巜悢娭悢揑偵懡偔側傞偺偱専弌晹傪椻憼屔撪偵擺傔傞偙偲偱偁偭偨丏偦偺戞2偼丆寁悢帋椏傪堦捈慄忋偵乮婡庬偵傛偭偰偼捈妏偵乯抲偐傟偨2杮偺PMT偵嫴傫偱抲偒丆2杮偺PMT傪摨帪偵嶌摦偝偣偨怣崋偩偗傪寁悢偡傞夞楬丆摨帪寁悢夞楬乮coincidence circuit乯傪嵦梡偡傞偙偲偱偁偭偨丏弶婜偺PMT偺暘夝帪娫乮憡師偄偱擖幩偟偨2偮偺曻幩慄傪2偮偲偟偰擣幆偡傞嵟抁帪娫乯偑挿偐偭偨偺偱丆2偮偺擬嶨壒偑摨帪偵擖幩偟偰乬婾寁悢accidental coincidence count乭偵側傝丆BG傪崅傔傞堦場偵側偭偰偄偨丏媄弍偺恑曕偵傛偭偰擬嶨壒偑彮側偔偟偐傕暘夝帪娫偑廫暘偵抁偄PMT偑擖庤偱偒傞傛偆偵側傝丆寁悢晹偺椻媝偼昁偢偟傕昁梫側偔側偭偨丏媡偵暘夝帪娫傪偁傑傝抁偔偡傞偲丆寀岝偺僄僱儖僊乕傪姰慡偵庢傝崬傓偙偲偑偱偒側偄偺偱丆嵟嬤偺憰抲偱偼PMT偺暘夝帪娫傪栺20 ns偵挷愡偟偰巊偭偰偄傞丏
摨帪寁悢夞楬傪捠夁偟偨怣崋偼丆怣崋偛偲偵弌椡偑崌嶼偝傟丆攇崅暘愅憰抲 multi channel analyzer乮MHA乯偱攇崅暘愅偝傟傞丏PMT偺揹巕憹攞棪偼堦掕偱傕丆MHA偵擖傞怣崋偺嫮搙偼丆偦偺兝夡曄偱兝慄偲偟偰曻弌偝傟偨僄僱儖僊乕丆敪岝岠棪乮僋僄儞僠儞僌偺掱搙乯丆兝夡曄偑婲偭偨埵抲乮PMT偺岝揹柺傪朷傓棫懱妏偼埵抲偵傛偭偰堎側傞乯側偳偵傛偭偰傑偪傑偪偱偁傞丏偐偔偟偰丆墶幉偵僠儍僱儖斣崋丆廲幉偵偦偺僠儍僱儖偱撉傒庢傜傟偨僷儖僗偺悢傪僾儘僢僩偡傞偲僷儖僗攇崅僗儁僋僩儖pulse height spectrum偑摼傜傟傞丏
Low BG LSC偱偼丆斈梡宆LSC偵懳偟偰師偺揰偑夵椙偝傟偰偄傞丏専弌晹偼丆摍妏搙偵攝抲偝傟偨3杮偺PMT偐傜側傞僙儞僞乕寁悢娗偲丆偙傟傪庢傝姫偔僾儔僗僠僢僋僔儞僠儗乕僞傪専弌婍偲偡傞僈乕僪寁悢娗偐傜峔惉偝傟偰偍傝丆椉寁悢娗傪摨帪偵嶌摦偝偣偨曻幩慄怣崋偼僇僢僩偝傟傞夞楬乮媡摨帪寁悢夞楬anti-coincidence circuit乯偱寢慄偝傟偰偄傞丏偙偺夞楬偵傛偭偰塅拡慄桼棃偺BG曻幩慄偼桳岠偵徚嫀偝傟傞丏傑偨丆Low BG LSC偱偼3杮偺PMT偑梡偄傜傟偰偍傝丆2杮偢偮3慻偺摨帪寁悢夞楬偵傛偭偰寢慄偝傟偰偍傝丆accidental coincidence count傪峏偵彫偝偔偟偰偄傞丏傑偨丆PMT傪2杮偐傜3杮偵偡傞偙偲偵傛偭偰丆僶僀傾儖撪偱偺敪岝傪50%傕懡偔懆偊傞偙偲偑偱偒傞偨傔丆斈梡宆偵斾傋偰乬僋僄儞僠儞僌偵嫮偄寁悢乭偑壜擻偵側偭偨丏
LSC偱偼丆奺帋椏偺僋僄儞僠儞僌偺嫮搙傪帵偡栚埨偲偟偰奜晹昗弨僠儍儞僱儖斾 (ESCR) 偑巊傢傟偰偄傞丏偙傟偼丆寁悢帋椏偵兞慄傪徠幩偟, 僐儞僾僩儞嶶棎偱惗偠傞擇師揹巕偺僗儁僋僩儖偺宍忬傪應掕偡傞偙偲偵傛偭偰媮傔傜傟偨抣偱丆偙偺抣偑彫偝偄傎偳僋僄儞僠儞僌傪嫮偔庴偗偰偄傞偙偲傪帵偡丏廬偭偰丆ESCR傪巜昗偵偟偰僌儖乕僺儞僌偟丆僌儖乕僾偛偲偵嵟揔僂僀儞僪僂偱寁悢偡傞偙偲傕偱偒傞丏BG抣偲ESCR偺娭學偵偮偄偰偼屻偱夝愢偡傞丏
奺帋椏丆奺婡庬偵傛傞兝慄攇崅僗儁僋僩儖
朻摢偱弎傋偨傛偆偵丆尰嵼梡偄傜傟偰偄傞LSC偼壗愮僠儍僱儖偲偄偆崅偄僄僱儖僊乕暘夝擻傪帩偮丆暘岝婍偲偟偰偺婡擻傕偁傢偣旛偊偨曻幩慄寁悢憰抲偱偁傞丏Fig. 3偼丆悈丆擜乮偄偢傟傕5 mL乯媦傃偦傟偧傟偵1 Bq偺 14C傪揧壛偟偨帋椏傪Low BG LSC媦傃斈梡宍LSC偱應掕偟偰摼傜傟偨攇崅暘晍嬋慄偺椺傪帵偡丏側偍丆1500 ch埲忋偼徣棯偟偰偁傞丏
傑偢拲栚偡傋偒偙偲偼丆兝慄攇崅僗儁僋僩儖偼僶僀傾儖偺僒僀僘偵傛偭偰旝柇偵堎側傞偙偲偱偁傞丏撪梕愊145 mL偺戝宆僶僀傾儖傪梡偄偨偲偒偵偼500 ch傑偱偱弌廔偭偰偄偨14C偺僷儖僗乮Fig.1乯偼丆昗弨僒僀僘僶僀傾儖偱偼800 ch 傑偱尰傟偰偄傞偙偲偱偁傞丏偡側傢偪丆昗弨僒僀僘僶僀傾儖偱偼丆戝宆僶僀傾儖偵斾傋偰攇崅僗儁僋僩儖偑崅攇崅懁偵庒姳僔僼僩偟偨忬懺偱寁悢偟偰偄傞偙偲偑暘偐傞丏

Fig. 3 Pulse height spectra of 5 mL human urine and related samples
晛捠丆14C偼丆壓尷慖暿揹埑傪悢keV偵忋尷揹埑傪14C 兝慄偺嵟戝僄僱儖僊乕156 keV偵愝掕偟偨丆B僂僀儞僪僂偲捠徧偝傟傞僂僀儞僪僂偱寁悢偝傟偰偄傞丏
傑偢丆悈偲擜傪 Low BG LSC 媦傃斈梡宍 LSC 偱應掕偟偰摼傜傟偨 A乣C 傪斾妑偡傞丏A 偼憰抲帺恎偺 BG乮machine noise乯偺僗儁僋僩儖偲娕橍偡偙偲偑偱偒傞丏C 偱偼丆慡椞堟偵搉偭偰寁悢偑 A 傛傝傢偢偐偵崅偄孹岦偑尒傜傟傞丏偙傟偼丆擜偵懚嵼偡傞 modern carbon 桼棃偺 14C (800 ch晅嬤傑偱丆F傪嶲徠)傪弶傔丆擜拞偵懚嵼偡傞撪場惈曻幩惈摨埵懱乮40K乯偵婲場偡傞傕偺偲峫偊傜傟傞丏摨偠擜傪 2 偮偺塼僔儞偱應掕偟偨 B 偲 C 傪斾妑偡傞丏C 偱偼慡椞堟偵傢偨偭偰寁悢偑掅偄丏摿偵50 ch埲壓偺寁悢偑尠挊偵掅壓偟偰偄傞丏偙偺帠幚偼丆媡摨帪寁悢夞楬偵傛偭偰崅僄僱儖僊乕塅拡慄偑嬌傔偰桳岠偵僇僢僩偝傟偰偄傞偙偲傪帵嵈偟偰偄傞丏
師偵丆1 Bq偺14C傪揧壛偟偨帋椏傪應掕偟偨D乣F傪斾妑偡傞丏D偱偼丆50 偐傜200 ch偵偐偗偰捀忋晹傪宍惉偟丆1500ch偵岦偗偰娚傗偐偵壓崀偟偰偄偔僗儁僋僩儖偵側偭偰偄傞丏悈帺恎偑偐側傝嫮偄僋僄儞僠儍乕偱偁傞丏擜偱偼丆僇儔乕僋儞僠儞僌偑壛傢傞偺偱峏偵嫮偄僋僄儞僠儞僌偑尰傟傞丏Low BG LSC 偱應掕偟偰摼傜傟偨F偱偼嫮搙偺僋僄儞僠儞僌偵傛偭偰僗儁僋僩儖慡懱偑掅攇崅懁偵埑弅偝傟偨宍偵側傝丆800 ch 埲崀偺怣崋嫮搙偼丆C偺憡摉偡傞椞堟偺偦傟偲傎傏摨偠偵側偭偰偄傞丏偙偺偙偲偼丆14C偺僷儖僗偼800 ch 傑偱偱傎傏姰慡偵撉傒廔傢偭偰偄傞偙偲傪帵嵈偟偰偄傞丏掅攇崅懁偵埑弅偝傟傞孹岦偼丆斈梡宆LSC偱應掕偟偰摼傜傟偨E偱偼峏偵尠挊偵尰傟偰偄傞丏Low BG LSC偱偼丆PMT傪3杮巊偭偰偄傞偺偱丆僶僀傾儖撪偱偺敪岝傪斈梡宆偵斾傋偰50%傕懡偔庢傝崬傫偱偄傞偙偲偑丆Low BG LSC偱偼乬僋僄儞僠儞僌偵嫮偄乭應掕傪壜擻偵偟偰偄傞偲愢柧偝傟傞丏
Fig. 3 E, F偐傜柧傜偐側傛偆偵丆5mL偺擜偱偼丆悈偵傛傞壔妛僋僄儞僠儞僌偺傒側傜偢僇儔乕僋僄儞僠儍乕傕嫮偔庴偗傞偙偲偵側傞丏僋僄儞僠儞僌傪庴偗偰偄傞帋椏偺應掕偵偍偄偰丆Eff 傪戝偒偔偡傞偨傔偵忋尷攇崅慖暿揹埑傪忋偘傞偲丆BG 寁悢傕崅偔側傞丏廬偭偰丆忋尷攇崅慖暿揹埑傪偳偙偵愝掕偡傞偐偑廳梫側壽戣偱偁傞丏曻幩擻偺應掕惛搙偼寁悢岠棪偺1忔丆BG抣偺1/2忔偵斀斾椺偟偰岦忋偡傞丏偦偙偱曻幩慄應掕婍乮朄乯偺惈擻斾妑偵偼 Eff 2/BG (figure of merit, FOM)偑梡偄傜傟偰偄傞丏FOM抣偑嵟戝偵側傞傛偆偵攇崅慖暿婍偺僂僀儞僪僂 (嵟揔僂僀儞僪僂丆optimal window) 傪愝掕偡傞偙偲偑娞梫偱偁傞丏嶲峫傑偱偵丆Fig. 3 D, F偵偼嵟揔僂僀儞僪僂偺埵抲偑帵偝傟偰偄傞丏
Table 1偼丆偄偢傟傕5mL偺奺庬偺寁悢帋椏傪B 僂僀儞僪僂偲嵟揔僂僀儞僪僂偱撉傒庢偭偨寁悢僨乕僞偱丆僂僀儞僪僂愝掕偺廳梫惈傪帵偡昞偱偁傞丏乮 乯撪偵梌偊傜傟偰偄傞Eff偼丆1Bq傪揧壛偟偨帋椏偺寁悢棪抣偺憹壛偐傜嶼弌偟偨丏[ ] 撪偵梌偊傜傟偰偄傞悢抣偼FOM抣偱偁傞丏
Table 1 丂The discriminator voltages of windows and counting rates

嵟揔僂僀儞僪僂偱寁悢偡傞偙偲偺廳梫惈
掅儗儀儖帋椏偺應掕偵偍偄偰LOQ傪寛傔傞偺偼BG帋椏偱娤嶡偝傟傞SD偺戝偒偝偱偁傞丏悈帋椏偵偮偄偰斾妑偡傞偲丆B僂僀儞僪僂偺Eff偼嵟揔僂僀儞僪僂偺偦傟傛傝傕偼傞偐偵崅偄偑丆BG傕崅偄丏偦偺寢壥丆嵟揔僂僀儞僪僂偱寁悢偟偨応崌偺LOQ偼3.3 mBq/mL丆B僂僀儞僪僂偱寁悢偟偨応崌偺偦傟偼6.2 mBq/mL偲側傞丏擜偵偮偄偰専摙偡傞偲丆嵟揔僂僀儞僪僂偱寁悢偟偨応崌偺LOQ偼8.5 mBq/mL丆B僂僀儞僪僂偱寁悢偟偨応崌偺偦傟偼13.2 mBq/mL偲側傞丏嵟揔僂僀儞僪僂偱寁悢偟偨応崌偺FOM抣偼偄偢傟傕栺2攞岦忋偟偰偄傞偙偲偼拲栚偡傋偒偙偲偱偁傞丏摨偠應掕憰抲丆摨偠帪娫偲楯椡傪偐偗側偑傜丆僂僀儞僪僂愝掕偺巇曽偵傛偭偰惈擻偑2攞傕岦忋偡傞偙偲傪嫮挷偟偰偍偔丏
嵟揔僂僀儞僪僂偱寁悢偡傞偙偲偺廳梫惈傪帵偡傕偆1偮偺椺傪丆擜拞撪場惈14C BG抣偺曄摦傪専摙偟偨尋媶乮Fig. 7乯偱徯夘偡傞丏
AMS偵娭偡傞懡偔偺憤愢偱偼丆AMS偺姶搙偼LSC偺1000攞偱偁傞偲徯夘偝傟偰偄傞丏嵟嬤丆僸僩偵14C昗幆栻暔傪搳梌偟丆擜拞偺14C傪AMS偱應掕偟偨媨壀傜偼LOQ 偲偟偰1 dpm/mL urine傪曬崘偟偰偄傞(7)丏 Low BG LSC傪梡偄丆嵟揔僂僀儞僪僂偱5 mL偺擜傪100暘娫寁悢偟偨応崌偺LOQ偼AMS偺 2攞偵岦忋偟偰偄傞丏崱夞丆LSC偵娭偟偰堦斒偵峫偊傜傟偰偄傞傛傝偼傞偐偵崅偄姶搙偑摼傜傟偨偺偼丆Low BG LSC傪梡偄偨偙偲丆帋椏検傪壜擻側尷傝戝偒偔偟偨偙偲丆嵟揔僂僀儞僪僂傪嵦梡偟偨偙偲側偳偵傛傞偲峫偊傜傟傞丏
丂
Fig. 4 A, B偵偼丆Low BG LSC媦傃斈梡宆LSC偱偦傟偧傟100暘娫, 10暘娫寁悢偟偨応崌偺寁悢棪抣偺捈慄惈傪恾帵偡傞丏杮恾偵偍偄偰丆Eff偼捈慄偺岡攝丆BG抣偼y幉偺愗曅偲偟偰梌偊傜傟傞丏

Fig. 4 Linearity of sub-Becquerel 14C (human urine 5 mL)
傑偢丆Fig. 4A偵偮偄偰峫嶡偡傞丏Low BG LSC偺BG寁悢偼5.3 cpm偱,斈梡宆偺14.1cpm偵斾傋偰栺3暘偺1偵掅壓偟偰偄傞丏傑偨丆Eff偼偦傟偧傟79.3 %,67.1% 偱偁傞丏曻幩慄應掕憰抲乮朄乯偺惈擻偼丆Eff2/BG偱梌偊傜傟傞FOM抣偵婎偯偄偰昡壙偝傟偰偄傞丏Fig. 4A偺僨乕僞偐傜Low BG LSC媦傃斈梡宆LSC偺FOM抣偼偦傟偧傟1177丆320偲嶼弌偝傟傞丏偡側傢偪丆Low BG LSC偱偼BG寁悢偑掅偔偟偐傕Eff偑崅偄偺偱3.7攞崅偄惈擻傪帩偭偰偄傞偙偲偵側傞丏
Fig. 4B偐傜傕摨偠寢榑偑摼傜傟傞丏Low BG LSC偺FOM抣乮1011乯偼丆斈梡宆LSC偺偦傟(284)偵斾傋偰3.6攞傕崅偄丏
Low BG LSC偺宱嵪岠壥
曻幩擻偺寁悢惛搙偼丏寁悢帪娫偺1/2忔偵斾椺偟偰岦忋偡傞丏Low BG LSC偑斈梡宍LSC偵斾傋偰3.6攞崅偄惈擻傪帩偭偰偄傞偲偄偆偙偲偼丆慜幰偵傛傞10暘娫寁悢偺惛搙偼屻幰偵傛傞100暘娫寁悢偺惛搙偵憡摉偡傞偲偄偆偙偲偱偁傞丏栻暔摦懺尋媶偵偼丆尋媶幰偺恖審旓丆幚尡摦暔偺峸擖丆帞堢旓丆昗幆栻暔偺峸擖旓丆摦暔幚尡旓丆攑婞暔張棟旓側偳偺傎偐偵挔曤偵寁忋偝傟側偄條乆側宱旓偑悡傫偱偄傞偲巚傢傟傞丏斈梡宆LSC傪Low BG LSC偵愗傝戙偊傞偙偲偼丆尋媶旓丆幚尡強梫婜娫側偳偼摨偠偱one rank 崅偄僨乕僞偑摼傜傟傞乮椺偊偽丆1敿尭婜掅擹搙傑偱捛愓偱偒傞乯偙偲傪丆偁傞偄偼1戜偺Low BG LSC偱丆寁悢惛搙傪堐帩偟偨傑傑10戜偺斈梡宆偺帋椏傪張棟偱偒傞偙偲傪堄枴偟偰偄傞丏偙傟傜傪憤崌揑偵峫偊傞偲丆斈梡宍LSC傪Low BG LSC 偵抲姺偡傞偙偲偼丆弶婜偺挻夁搳帒傕抁婜娫撪偵夞廂偱偒傞偙偲偼柧傜偐偱偁傞丏
兝慄攇崅僗儁僋僩儖傕採帵偟傛偆丏
LSC偲偄偊偽寁悢棪抣 cpm偺傒傪庢傝忋偘丆偦偺寁悢偑偄偐側傞忬嫷偺傕偲偵側偝傟偨傕偺偐傪尵媦偟偰偄傞榑暥偼奆柍偱偁傞丏MD偱偼丆嫮偔僋僄儞僠儞僌傪庴偗偰偄傞帋椏傪埖偆偙偲偵側傞丏偟偨偑偭偰丆兝慄攇崅僗儁僋僩儖傕採帵偟丆嵟揔忦審偱寁悢偝傟偰偄傞偙偲傪棫徹偟偰偍偔傋偒偱偁傞丏堦椺傪嫇偘傞丏Fig. 5偼丆Low BG LSC偱寁悢棪抣偺捈慄惈傪尒偨Table 1偺僨乕僞偐傜撉傒弌偟偨兝慄攇崅僗儁僋僩儖偱偁傞丏拲栚偡傋偒偙偲偼丆0.03Bq 偺14C傪揧壛偟偨帋椏乮0.36 dpm/mL urine乯偱婛偵BG帋椏偲桳堄偺嵎偑擣傔傜傟偰偄傞偙偲偱偁傞丏偙偺応崌丆寁悢棪偲嫟偵丆偙偺僗儁僋僩儖僨乕僞傪偮偗壛偊傞偙偲偵傛偭偰僨乕僞偺怣棅惈偼堦抜偲崅傑傞偲巚傢傟傞丏昅幰偼丆崱屻偼BG帋椏傪娷傔偰媍榑偺尞偵側傞帋椏偵偮偄偰偼寁悢棪僨乕僞偲嫟偵僗儁僋僩儖僨乕僞傕採帵偡傞偙偲傪採埬偡傞丏
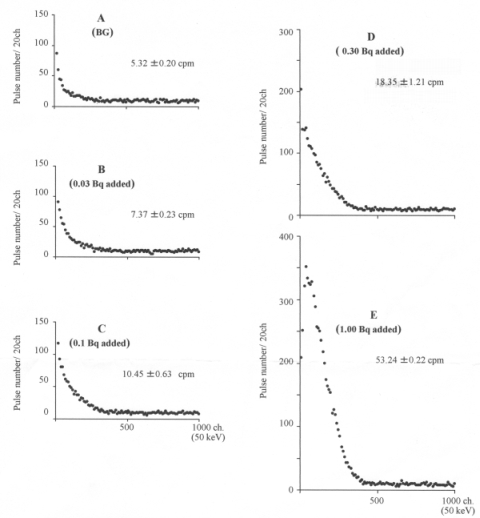
Fig. 5丂Pulse height spectra of sub-becquerel 14C乮human urine 5 mL乯
Low BG LSC偵偍偗傞慖戰巿
Low BG LSC偼娐嫬曻幩擻偺應掕傪栚揑偵奐敪偝傟丆巊傢傟偰偄傞LSC偱丆栻暔摦懺尋媶偺暘栰偵偍偄偰慡偔偺怴嶲幰偱偁傞丏MD偵偍偄偰丆Low BG LSC偺巊偄曽偵偼丆戝宆僶僀傾儖乮撪梕愊145 mL乯傪巊梡偡傞曽朄丆傾僞僢僠儊儞僩傪梡偄偰昗弨僒僀僘僶僀傾儖乮撪梕愊20 mL乯偱應掕偡傞曽朄丆帋椏傪擱從偟偰惗惉偟偨擇巁壔扽慺傪傾僙僠儗儞宱桼儀儞僛儞偵曄姺偟丆昗弨僒僀僘僶僀傾儖偱應掕偡傞曽朄乮9乯偺3偮偺慖戰巿偑偁傞丏
尰嵼丆巗斕偝傟偰偄傞Low BG LSC偼戝宆僶僀傾儖偵懳墳偱偒傞傛偆偵愝寁偝傟偰偍傝丆堦搙偵憰揢偱偒傞帋椏悢偼25屄偱偁傞丏偙偺僒僀僘偱偼僔儞僠儗乕僞徚旓検偑戝偒偄偙偲丆寁悢夁掱偵偍偗傞斈梡宆LSC偲偺屳姺惈偑側偄偙偲媦傃寁悢抣傪捈愙斾妑偱偒側偄偙偲側偳偐傜丆昅幰傜偼傾僞僢僠儊儞僩傪梡偄偰昗弨僒僀僘僶僀傾儖偱應掕偟偰偄傞丏僱僢僋偼廳幷暳偑昁梫側應掕幒偺梕愊偱偁傞丏昗弨僒僀僘僶僀傾儖愱梡側傜丆傎傏摨偠幷暳嫮搙傪堐帩偟偰丆堦搙偵50屄憰揢偱偒傞婡夿傕愝寁壜擻偲暦偄偰偄傞丏堦搙偵憰揢偱偒傞帋椏悢偑彮側偄偙偲偑丆斈梡宆LSC傪巊偄姷傟偨幰偵偲偭偰偼晄枮偲傕峫偊傜傟傞丏昅幰偼師偺2偮偺帠忣偐傜丆嵎偟摉傝尰懚偺宆偱枮懌偟偰偄傞丏僸僩偺幚尡偱偼丆摦暔幚尡偵斾傋偰帋椏偼挊偟偔尩慖偝傟丆堦恖摉傝偺帋椏悢偼偣偄偤偄慡晹偱25帋椏偲峫偊傜傟傞丏傑偨婱廳側帋椏傪10暘寁悢偱廔傢傞偺偼傕偭偨偄側偄榖偱偁傞丏寢嬊丆1旐尡幰偐傜弌傞堦楢偺帋椏偺悢偑25偵側傞傛偆偵幚尡寁夋傪棫偰丆1帋椏30乣100暘娫寁悢偟偰1乣2擔娫偱寁悢嶌嬈偑廔傢傞偺偑崌棟揑側偲偙傠偱偁傞偲峫偊傞丏傑偨丆尰嵼恑峴拞偱偁傞偑丆應掕懳徾傪僾儔僘儅傗戝曋偵奼挘偟偨応崌丆昗弨僒僀僘僶僀傾儖偱偳偙傑偱帋椏僒僀僘傪戝偒偔偱偒傞偐晄徻偱, 応崌偵傛偭偰偼戝宆僶僀傾儖傪巊傢偞傞傪偊側偄壜擻惈傕偁傞丏
Low BG LSC偵傛傟偽丆10暘娫寁悢偱斈梡宆LSC偺100暘娫寁悢偺惛搙偑摼傜傟傞丏 Low BG LSC偺挿強偑擣傔傜傟偰丆Low BG LSC偑LSC偺庡棳偵側傝丆椺偊偽丆儔僕僆HPLC偺off-line寁悢側偳偵傕峀偔梡偄傜傟傞傛偆偵側偭偨応崌偵偼丆昗弨僒僀僘僶僀傾儖愱梡偺婡庬偺巗応惈偑弌偰偔傞偲巚傢傟傞丏側偍丆Low BG LSC偑儔僕僆HPLC偺off-line寁悢朄偲偟偰桳朷側偙偲偵偮偄偰偼屻弎偡傞丏昗弨僒僀僘僶僀傾儖愱梡偺婡庬偱偼丆岝揹巕憹攞娗傪僶僀傾儖偵傛傝枾拝偱偒丆寀岝傪傛傝崅偄婔壗妛揑岠棪偱懆偊傞偙偲偑偱偒傞偺偱丆偦傟偩偗岲忦審偱寁悢偱偒傞偺偱偼側偄偐偲婜懸偟偰偄傞丏
峏偵崅偄LOQ傪婜懸偡傞側傜丆帋椏傪擱從偟偰惗惉偟偨擇巁壔扽慺傪傾僙僠儗儞宱桼儀儞僛儞偵曄姺偟偰應傞曽朄偱偁傞乮9乯丏偙偺曽朄偱偼丆椺偊偽6g偺扽慺偐傜6.5g偺儀儞僛儞偑摼傜傟傞偙偲偵側傝丆儀儞僛儞帺恎偼搒崌偺椙偄僔儞僠儗乕僞梟攠偱偁傞偺偱傛傝崅偄Eff 偱14C傪寁悢偡傞偙偲偑偱偒傞丏崱擔傑偱偵傢偑崙偵偼儀儞僛儞崌惉憰抲偑30戜傎偳桝擖偝傟偰偍傝丆儓儌僊側偳傪儅乕僇乕僾儔儞僩偵偟偰尨巕楩偐傜偺儕乕僋14C傪儌僯僞乕偟偰偄傞丏偙偺曽朄傪嵦梡偡傟偽1擔偺暢曋偺廫暘偺1傪應傞偙偲偑偱偒傞丏偙傟偙偦媶嬌偺儅僗僶儔儞僗帋尡朄偱偁傞丏
MD偵偍偗傞Low BG LSC偲 AMS偺斾妑
10擭傎偳慜偐傜丆惗懱帋椏拞偺掅儗儀儖14C 偺應掕朄偲偟偰AMS偑採埬偝傟丆AMS偑MD偵偍偗傞the one and only method偺傛偆側堄尒偑峀偑偭偰偄傞丏AMS偱偼丆僌儔僼傽僀僩偵偟偨帋椏傪僀僆儞壔偟丆幙検暘愅娗偱扽慺偺摨埵懱傪暘棧偟丆 12C偲 13C僀僆儞偼僼傽儔僨傿僇僢僾偱僀僆儞揹棳傪應掕偟偰検傪媮傔丆14C 偼敿摫懱専弌婍偵擖幩偝偣偰14C 偺屄悢傪寁應偟偰偄傞丏1屄偺14C尨巕妀偑1暘娫偵曵夡偡傞妋棪偼栺6亊109暘偺1偱偁傞丏乬嬌傔偰掅偄妋棪偱婲偭偰偄傞曵夡傪悢偊傞傛傝傕14C偺屄悢傪捈愙悢偊傞AMS偺曽偑姶搙偺椙偄寁應偑偱偒傞偼偢偱偁傞乭偲偄偆偺偑AMS偺弌敪揰偱偁傞(3)丏偨偟偐偵丆婬側妋棪偱婲偙偭偰偄傞曵夡傪悢偊傞傛傝傕14C 偺屄悢傪應偭偨曽偑姶搙偺椙偄應掕偑偱偒偦偆偵嶖妎偡傞偑丆偙偺敪憐偵偼丆婔偮偐偺尒棊偟偑偁傞丏
傑偢丆LSC偺sample size偑寘堘偄偵戝偒偄乮晛捠丆1000攞偲尒愊傕偭偰椙偄乯偙偲偱偁傞丏LSC偱偼丆寁悢帪娫撪偵寁悢帋椏撪偱婲偭偰偄傞14C 偺曵夡偺70乣80亾傪懆偊偰偄傞丏AMS偱偼丆僌儔僼傽僀僩壔偝傟傞廂棪丆14C僀僆儞壔廂棪乮曻幩壔暘愅偵偍偗傞妀斀墳抐柺愊偵憡摉乯丆14C僀僆儞偑専弌婍傑偱摓払偡傞廂棪側偳偑栤戣偵側傞丏僌儔僼傽僀僩壔廂棪偼100%偲尒愊傕偭偰椙偄偱偁傠偆偑丆懠偺2偮偵偮偄偰晄柧偱偁傞丏
栤戣偼14C偺僀僆儞壔廂棪偱偁傞丏14C尨巕偺僀僆儞壔偺夁掱偼丆拞惈巕偵傛傞曻幩壔暘愅activation analysis偺夁掱偵帡偰偄傞丏14C僀僆儞偺惗惉検偼丆14C 偺懚嵼斾乮栺昐壄暘偺1%乯乮4乯丆僀僆儞壔棻巕懇枾搙乮particles/mm2/s乯丆14C偺僀僆儞壔廂棪丆媦傃僀僆儞壔帪娫乮亖寁應帪娫乯偵斾椺偡傞丏曻幩壔暘愅偱偼摨偠尦慺偱傕摨埵懱偵傛偭偰妀斀墳抐柺愊偵戝偒側嵎偑偁傞偙偲偑抦傜傟偰偄傞偑丆C偺3偮偺摨埵懱偵偼僀僆儞壔廂棪偵嵎偑偁傞偲偼峫偊傜傟側偄丏偙偺拞偱栤戣偵側傞偺偼14C 偺懚嵼斾偑嬌抂偵彫偝偄偙偲偱偁傞丏Low BG LSC偱偼sample size傪戝偒偔偡傞丆寁悢帪娫傪墑挿偡傞側偳偺梋抧偑偁傞偑丆AMS偱偼偙傟傜偺帺桼搙偼傎偲傫偳側偄偲峫偊傜傟傞丏
傑偨丆専弌宯偵擖偭偰偒偨傕偺傪寁検偟偰偄傞幙検暘愅朄偵偼屌桳偺尰徾偱偁傞丆儊儌儕乕偺栤戣偐傜摝傟傞偙偲偑偱偒側偄丏偙偺応崌偵偼AMS帋椏挷惢憰抲偵偍偗傞儊儌儕乕傕峫椂偟側偗傟偽側傜側偄丏傑偨丆儊儌儕乕偼 乬positive memory乭偩偗傪峫偊偑偪偱偁傞偑丆BG帋椏偑丆師偺帋椏偺抣傪掅偔偡傞乬negative memory乭傕峫椂偟側偗傟偽側傜側偄丏幙検暘愅寁傪巊偭偨宱尡偐傜丆儊儌儕乕岠壥偵婲場偡傞岆嵎傪旔偗傞偨傔偵偼丆應掕帋椏偺挷惢僗僥僢僾傪娷傔偰1偮偺帋椏傪3夞應掕偟丆儊儌儕乕偑柍偔側偭偨偙偲傪妋擣偟偰偦偺帋椏偺嵟廔應掕抣偲偡傞怲廳偝偑媮傔傜傟傞丏偡側傢偪丆帋椏挷惢憖嶌傕娷傔偰丆幚嵺偵偼3攞傕懡偔偺帋椏傪張棟偟側偗傟偽側傜側偄偲偄偆偙偲偱偁傞丏應掕偼丆掅偄曽偐傜崅偄曽傊峴偆偺偱儊儌儕乕偼栤戣偵側傜側偄偲偄偆偺偼丆negative memory傪峫偊傞偲嫋偝傟側偄丏偙傟偵懳偟偰LSC偱偼儊儌儕乕偵婲場偡傞栤戣偼懚嵼偟側偄丏
AMS偺sample size偑嬌傔偰彫偝偄偙偲傕栤戣偱偁傞丏崱丆暘巕拞偺1偐強傪柍扴懱14C 偱昗幆偝傟偨1 n mol偺昗幆栻暔乮昗幆埵抲埲奜偼慡偰dead carbon偐傜側傞乯傪巊偭偰MD傪幚巤偟偨応崌傪峫偊偰傒傛偆丏僸僩偼1擔摉傝10 mol偺扽慺傪愛庢偟偰偄傞偲壖掕偡傞偲丆14C偼100壄攞検偺 modern carbon乮13.56 dpm/g傪娷傓乯偱婓庍偝傟偨忬懺偱應掕偝傟傞偙偲偵側傞丏AMS偱偼帋椏偐傜傢偢偐0.1 m mol C傪嵦偭偰14C傪掕検偟側偗傟偽側傜側偄丏偙偺応崌丆慡懱傪惛妋偵戙昞偡傞應掕帋椏傪挷惢偡傞偙偲偼乮摿偵屌宍攔煏暔偱偼乯嬌傔偰斚嶨側嶌嬈偵側傞偲峫偊傜傟傞丏Sample size偑偙傟傛傝100乣1000攞傕戝偒偄Low BG LSC偱偼偙偺傛偆側栤戣偼婲傜側偄丏AMS偺昗弨揑側應掕帋椏偲偟偰1乣5 dpm 14C /mg C偑嫇偘傜傟偰偄傞丏偙偺帋椏偼丆乮LSC偺sample size偑AMS偺100攞偲偟偰乯LSC偱偼100乣500 dpm/sample偺帋椏偵憡摉偡傞丏偙偺曻幩擻儗儀儖偺帋椏偼丆斈梡宆LSC傪巊偭偰10暘娫寁悢偡傟偽廫暘側惛搙偑摼傜傟傞丏僸僩擜偺BG偼1.5 dpm/mL慜屻偱偁傞丏昅幰傜偼丆5 mL偺擜傪帋椏偲偡傞応崌偵偼丆1 mL 擜摉傝0.36乣12.00 dpm 偺14C傪揧壛偟偨帋椏偱捈慄惈傪専摙偟偰偄傞丏偙偺傛偆側棟桼偐傜丆AMS偺昗弨揑側應掕帋椏偲偟偰0.01乣0.05 dpm 14C /sample偺帋椏傪梡偄傞傋偒偱偁傞丏
應掕帋椏偺挷惢憖嶌偑埑搢揑偵娙扨偱丆岆嵎梫場偑傎偲傫偳懚嵼偟側偄偙偲傕Low BG LSC朄偺挿強偱偁傞丏應掕帋椏偺挷惢夁掱偱LSC偱偼曻幩擻偵傛傞墭愼偩偗傪拲堄偡傟偽椙偄偑丆AMS偱偼曻幩擻偵傛傞墭愼偺傒側傜偢dead carbon偵傛傞婓庍傕拲堄偟側偗傟偽側傜側偄丏偙傟傜偺2偮偵敽偆岆嵎偺塭嬁偼丆帋椏偺14C検暲傃偵帋椏僒僀僘偵媡斾椺偟偰戝偒偔側傞偲峫偊傞偺偑懨摉偱偁傞丏暋嶨側帋椏挷惢夁掱偱丆偙傟傜2偮偺岆嵎梫場傪偄偐偵娔帇偡傞偐擄偟偄壽戣偱偁傞偲峫偊傜傟傞丏
傑偨丆扽慺偼丆摨埵懱懚嵼斾偺曄摦偑戝偒偄尦慺偱偁傞偙偲傕栤戣偱偁傞丏妀壔妛偱偼丆15N傗18O偺摨埵懱懚嵼斾偼桳岠悢帤4寘丆13C偺摨埵懱懚嵼斾偑埨掕偟側偄偺偱桳岠悢帤3寘偱昞帵偡傞偙偲偵側偭偰偄傞丏傾僀僜僩乕僾庤挔9斉乮擔杮傾僀僜僩乕僾嫤夛乯偱13C偺懚嵼斾偲偟偰嫇偘傜傟偰偄偨1.10偼丆10斉偱偼1.07偵曄峏偵側偭偨丏 14C偺懚嵼斾偵偮偄偰偼偁傑傝抦傜傟偰偄側偄偑丆13C偲摨條側曄摦偑偁傞偲峫偊傞偺偑懨摉偱偁傞丏廬偭偰丆modern carbon偵偍偗傞14C偺懚嵼斾偼堦掕抣偱偁傞偲偟偰14C検傪嶼弌偡傞偙偲偼婋尟偱偁傞丏
AMS偵娭偡傞暥專偱偼椺奜側偔AMS偺姶搙偼LSC偺1000攞偲婰嵹偝傟偰偄傞偑丆姶搙偼丆偦偺庤朄偱應掕壜擻側検傪扨埵検偵姺嶼偟偨抣偱斾妑偡傞傋偒偱偁傞丏傑偨丆LSC偺姶搙偼丆婡夿偺宆幃丆帋椏偺検丆寁悢帪娫丆攇崅慖暿偺巇曽側偳偵傛偭偰戝偒偔曄摦偡傞偺偱丆偙傟傜傪峫椂偟側偄斾妑偼柍堄枴偱偁傞丏AMS偑傛傝揔偟偰偄傞偺偼丆嵦庢帋椏検偑嬌抂偵惂尷偝傟偰偄傞帋椏丆椺偊偽峫屆妛帒椏偺擭戙應掕偵懳偟偰偱偁傞丏偙偺応崌偵偼modern carbon偵傛傞婓庍偑側偔丆摨埵懱懚嵼斾乮偡側傢偪丆柍師尦偺抣乯偩偗傪應傟偽椙偄偐傜偱偁傞丏
摑寁曄摦傪晅婰偱偒側偄AMS偼曻幩擻應掕朄偺巗柉尃偼摼傜傟側偄丏
帺慠壢妛偵偍偄偰師尦偼嵟傕婎慴揑側帠崁偱偁傞丏暔幙検偺SI扨埵偼mol丆曻幩擻偺SI扨埵偼s-1丂偱梌偊傜傟傞儀僋儗儖Bq偁傞丏帺慠壢妛偵偍偗傞晛捠偺幚尡偱偼梕堈偵mol偵揮姺偱偒傞暔棟尰徾傪庤偑偐傝偵幚尡偑恑傔傜傟偰偄傞偺偱師尦偑栤戣偵側傞偙偲偼側偄丏偟偐偟丆AMS偵傛傞儅僗僶儔儞僗帋尡偱偼丆搳梌偼曻幩擻偺師尦丆寁應偼暔幙検偱丆僶儔儞僗僔乕僩偼曻幩擻偵婎偯偄偰嶌惉偡傞偙偲偵側傞丏曻幩擻偲暔幙検偼師尦偺堎側傞暔棟検偱憡屳偵曄姺偱偒側偄丏
Bq偼丆mol偲堎側偭偰摑寁曄摦傪敽偆暔棟検偱偁傞丏曻幩擻偼夡曄偵傛偭偰帪帪崗乆尭悐偟偰偄偔抣偱偁傝丆傑偨掅儗儀儖曻幩擻偺帋椏偱偼扨埵帪娫摉傝偺夡曄悢乮dpm乯偼乮應掕偑惓偟偔峴傢傟偰偄偰傕乯摑寁曄摦傪敽偆抣偱偁傞丏乮14C偺敿尭婜偼丆幚尡婜娫偺帪娫偵斾傋偰廫暘偵挿偄偺偱偦偺尭悐偼柍帇偟偰嵎偟巟偊側偄丏乯偙偺傛偆側帠忣偐傜丆曻幩擻寁悢朄偱偼丆憤寁悢偵 亇 憤寁悢偺1/2忔傪晅婰偟偰丆偦偺寁悢偑偳偺偔傜偄偺摑寁曄摦偱側偝傟偨偐傪帵偡偙偲偵側偭偰偄傞乮擔杮傾僀僜僩乕僾嫤夛偺傾僀僜僩乕僾庤挔嶲徠乯丏偙傟偵懳偟偰丆埖偭偰偄傞尨巕傗暘巕偺悢偼揤暥妛揑側悢偱偁傞偺偱丆乮幚尡岆嵎偵敽偆曄摦偑偁偭偰傕乯mol偼摑寁曄摦傪敽傢側偄暔棟検偲偟偰埖傢傟偰偄傞丏廬偭偰丆AMS偱摼傜傟偨抣偺摑寁曄摦傪偳偺傛偆偵張棟偡傞偐丠傕偟偦傟偑偱偒側偄側傜丆搳梌検傪娷傔偰堦娧偟偰mol検偱採帵偡傞傋偒偱偁傞丏偳偆偟偰傕Bq傗 dpm偱採帵偣偞傞傪摼側偄側傜丆偄偐側傞夁掱偱mol傪偙傟傜偺扨埵偵曄姺偟偨偐丆傑偨偳偺偔傜偄偺摑寁曄摦偱寁應偝傟偰偄傞偐傪戞嶰幰偵傕僼僅儘僂偱偒傞傛偆偵偡傞傋偒偱偁傞丏傑偨丆偙偺応崌偵偼丂equivalent, obtained by AMS丆estimated by AMS etc 偲偄偆廋忺岅偑昁梫偵側傞偺偱偼側偄偐偲峫偊傞丏 AMS偱摼傜傟偨14C 検乮儌儖乯偼摑寁曄摦傪敽傢側偄抣偱偁傞偑丆Bq傗 dpm偼摑寁曄摦傪敽偆暔棟検偱偁傞丏廬偭偰丆偄偭偨傫mol検傪偙傟傜偺抣偱昞帵偡傞偲丆埲屻偼慡偰摑寁曄摦傪擮摢偵偍偄偰撉傑傟傞偲偄偆婏柇側偙偲偵側傞丏
AMS偺榑暥偵偼丆椺偊偽0.01dpm偲偄偆旕忢偵掅偄抣偑搊応偡傞偑丆摑寁曄摦偲偄偆娤揰偐傜偙傟偼棟夝偵嬯偟傓抣偱偁傞丏嬌傔偰幚嵺揑側働乕僗偵偮偄偰峫偊偰傒傛偆丏柍尷夞悢LSC偱應掕偟偰丆1dpm 14C /mL urine偲偄偆抣偑摼傜傟偨擜1mL傪1丆10丆100暘娫寁悢偟偨応崌偺dpm抣偼摑寁曄摦傪晅偗偰丆偦傟偧傟
1.00亇1.00 dpm丆1.00亇0.32 dpm丆1.00亇0.10 dpm
偱梌偊傜傟傞丏偙偺応崌丆1.00 dpm偼彫偝偄抣偱偁傞偑丆摑寁曄摦傪偮偗傞偙偲偵傛偭偰偳偺偔傜偄怣棅偺偍偗傞抣偱偁傞偐偑暘偐傞丏傑偨丆偙偺帋椏偱傕100暘娫傕寁悢偡傟偽傑偢傑偢偺惛搙偑摼傜傟傞偙偲偑暘偐傞丏
傑偨丆LSC偱偼sample size傪戝偒偔偡傞偙偲偵傛偭偰摑寁曄摦傪峏偵彫偝偔偡傞偙偲偑偱偒傞丏偡側傢偪丆摨偠帋椏傪10mL偲傝丆1丆10丆100暘娫寁悢偟偨応崌偺dpm/mL抣偼師偺傛偆偵側傞丏
1. 00亇0.32 dpm丆1.00亇0.10 dpm丆1.00亇0.032 dpm
偡側傢偪丏LSC偱偼寁悢帪娫傪墑偽偡偙偲偲sample size傪戝偒偔偡傞偙偲偵傛偭偰拝幚偵摑寁曄摦傪彫偝偔偱偒傞偙偲偑暘偐傞丏
偙偺帋椏傪AMS偱應掕偟偨偲偟傛偆丏傑偢丆AMS偱偼寁悢帪娫偺忣曬傪慻傒崬傓偙偲偑偱偒側偄丏傑偨丆AMS偺sample size傪10兪L偲偡傞偲丆偙偺帋椏偼0.01dpm/sample偲側傝丆偙偺帋椏偺摑寁曄摦傪媍榑偡傞偙偲帺懱偑旕尰幚揑偲偄偆偙偲偵側傞丏 LSC偱偼寁悢帪娫偺墑挿丆sample size偺奼戝偵傛偭偰掕検尷奅傪奿抜偵岦忋偱偒傞偑丆AMS偱偼偦偺傛偆側偙偲偼偱偒側偄丏
掅儗儀儖曻幩擻傪埖偆榑暥偱偼丆幚尡偺晹偺曻幩擻應掕偺崁偱巊梡偟偨僔儞僠儗乕僞丆BG寁悢丆寁悢帪娫傪婰嵹偟丆偳偺偔傜偄偺摑寁曄摦偱幚尡偝傟偰偄傞偐偑暘偐傞傛偆偵偟偰偍偔偙偲偵側偭偰偄傞丏摑寁曄摦傪晅婰偱偒側偄應掕朄偼曻幩擻偺應掕朄偲偟偰偺巗柉尃偼摼傜傟側偄偲峫偊傞偺偑懨摉偱偁傞丏廬偭偰丆AMS偵傛傞MD偱偼丆搳梌丆帋椏偺應掕丆僶儔儞僗僔乕僩偺嶌惉偺慡僗僥僢僾傪mol検偱峴偆傋偒偱偁傞偲峫偊傞丏
AMS偲 LSC偺應掕抣偺憡娭惈傪0乣10000 dpm偵傢偨偭偰専摙偟丆椉幰偺憡娭惈偼椙岲偱偁傞偲曬崘偝傟偰偄傞丏偙偺曻幩擻儗儀儖偼抂憢宍GM寁悢娗偱傕應傟傞儗儀儖偱偁傞丏憡娭惈偼丆惗懱帋椏偱丆傕偭偲掅儗儀儖偺帋椏丆椺偊偽0乣10dpm/mL urine傪梡偄偰専摙偡傞傋偒偱偁傞丏 昅幰偼丆AMS偺惈擻偵嫮偄娭怱傪帩偭偰偄傞丏椉應掕朄傪斾妑偡傞偨傔偵丆偙偺復偵採帵偟偨Table 1, Fig.4, Fig. 5偵懳墳偡傞僨乕僞傪AMS偱傕憗偄帪婜偵採帵偟偰捀偒偨偄偲峫偊偰偄傞丏
岆嵎榑偐傜偄偭偰傕Low BG LSC偼偼傞偐偵桳棙偱偁傞丏偙偺曽朄偱偼丆帋椏拞偺14C偺寁悢偩偗傪媮傔傟偽栚揑傪払偡傞丏AMS偱偼丆14C乮僷儖僗悢乯丆12C傑偨偼13C乮揹棳抣乯丆憤扽慺乮儌儖検乯偺俁偮偺丆慡偔堎側傞暔棟検傪媮傔側偗傟偽側傜側偄丏偙傟傜偑丆偳偺偔傜偄偺岆嵎偱應掕偝傟偰偄傞偐柧偵偝傟偰偄側偄偑丆偦傟偧傟偵1%偺憡懳岆嵎傪敽偆偲偟丆嵟彫擇忔朄偱憤岆嵎傪寁嶼偡傞偲偼栺1.7%偵払偡傞偙偲偵側傞丏
傕偆1偮栤戣偵側傞偺偼敿摫懱専弌婍偱懆偊偰偄傞14C僀僆儞偺屄悢偺栤戣偱偁傞丏乬AMS偼14C 偺屄悢傪悢偊傞庤朄偱偁傞丏偟偨偑偭偰丆婬偵偟偐婲傜側偄曵夡悢傪悢偊傞曽朄傛傝傕丆AMS偼崅姶搙偺偼偢偱偁傞乭偲偄偆偺偑丆AMS偺崅姶搙惈傪庡挘偡傞尨揰偵側偭偰偄傞丏偦傕偦傕尨巕1屄丆1屄傪悢偊傞曽朄偼懚嵼偟側偄丏偙偺栤戣傪丆偙偺暘栰偵偍偗傞AMS 偺僷僀僆僯儎偱偁傞 Garner傜偺榑暥乮12乯偺僨乕僞傪嶲峫偵偟偰峫嶡偟偰傒傛偆丏側偍丆1dpm偼6亊109屄偺14C偵憡摉偡傞丏儌僨儖偲偟偰丆AMS偱偼1 dpm/0.1 mmol carbon偺帋椏傪丆Low BG LSC偱偼 1 dpm/1 mL urine 5 mL傪100暘娫寁應偡傞応崌傪峫偊傞丏Garner榑暥偱偼丆14C僀僆儞偼彮側偔偲傕1000屄傪寁應偡傞偲弎傋偰偄傞偺偱丆AMS偺寁應帪娫偼丆1000屄偺14C僀僆儞偑専弌婍偵擖幩偡傞帪娫偲偡傞丏AMS偺帋椏偵偼丆6亊1019屄偺扽慺尨巕偺拞偵6亊109屄偺14C偑娷傑傟偰偄傞偙偲偵側傞丏偡側傢偪丆寁應偟偰偄傞偺偼帋椏拞偵懚嵼偡傞14C偺6昐枩暘偺1偵夁偓側偄偲偄偆偙偲偱偁傞丏Low BG LSC偺寁悢岠棪偼80%慜屻偱偁傞偺偱丆慜婰偺儌僨儖帋椏偱偼400僇僂儞僩傪梌偊傞偙偲偵側傞丏Low BG LSC偺帋椏僒僀僘偼AMS偺100乣1000攞傕戝偒偄偙偲偲丆寘堘偄偵挿偄帪娫寁應偱偒傞偙偲傪峫偊傞偲丆幚梡揑側帋椏偱丆14C偺曵夡偺妋棪偑彫偝偄偙偲偼姰慡偵挔徚偟偵側傞丏
BG抣傪2攞偵偡傞曻幩擻傪傕偭偰乬桳堄偺曻幩擻乭偲偟偰偄傞尋媶幒偑懡偄丏僸僩擜偺14C BG偼1dpm/mL慜屻偱偁傞偐傜丆昅幰傜偼偙偺擹搙傪拞怱偵偟偰専検慄傪専摙偟偰偄傞乮Fig. 4,5嶲徠乯丏Modern carbon偵偼13,56dpm14C /g carbon偑娷傑傟偰偄傞丏AMS偺帋椏僒僀僘偼0.1 mmol偱偁傞偐傜丆0.016 dpm 14C /sample 慜屻偺帋椏偵偮偄偰捈慄惈傪専摙偡傞傋偒偱偁傞丏
AMS偑偦偺埿椡傪敪婗偱偒傞偺偼丆帋椏偺嵦庢検偑嬌抂偵惂尷偝傟傞廳梫暥壔嵿偺carbon dating乮偙偺応崌偵偼丆14C偲12C偺儌儖斾偩偗偑栤戣偵側傞乯傗偁傞庬偺柶塽暘愅乮modern carbon検偑彫偝偄乯偺応崌偱偁傞偲昅幰偼峫偊傞丏 carbon dating 偵偍偄偰傕桳婡暔偺懡偄帋椏偱偼Low BG LSC偑桳棙偲偄傢傟偰偍傝丆嵟嬤偱偼丆僈僜儕儞拞偺僶僀僆擱椏偺娷検偑Low BG LSC偱庤寉偵應傜傟偰偄傞丏
|





